-
发货地址:上海金山石化
信息编号:167722233,公司编号:14235332
产品规格:2
产品数量:2345.00 个
包装说明:3
产品单价:面议
官方网址:http://sungofda.cn.b2b168.com/
- 13818104617 袁小姐
- 留言数:12人
- 查看数:785人
办理TUV机构的MDRCE认证需要做哪些检测?-需要什么材料
- 相关产品:
MDRCE认证
上海沙格企业管理咨询有限公司
会员 9 年
- 所在区域:上海金山石化
- 经营性质:外商独资企业
- 企业类型:商业服务
- 注册地:上海市金山区
- 主营产品:CE,MDR认证,MDR,CE认证,IVDR,欧代,EU2017/745认证,2017/746,EC,REP,CE技术文件,CE第四版临床评估报告.SUNGO,EN,455,UK,EN12184,清洗验证,FDA验厂
- 企业已认证
- 个人实名未认证
- 产品分类
-
FDA验厂
CE第四版临床评价报告
MHRA注册/欧盟授权代表
欧盟自由销售证书
医疗器械单一体系审核MDSAP
MDR CE认证
欧盟授权代表
US Agent,FDA美国代
美国FDA注册/认证
MDR EU2017/745认证
MDEL注册
- 商家其他产品
- “办理TUV机构的MDRCE认证需要做哪些检测?-需要什么材料”详细信息
咨询范围:2咨询类型:4服务项目:3品牌:4
SUNGO办理:
1:欧盟MDR CE,欧盟授权代表,欧盟注册
2:美国FDA注册,FDA510K
3:国内的医疗器械注册证和生产许可证
4:加拿大的MDEL注册
5:ISO13485咨询和认证
1)提供欧盟授权代表,授权在标签和说明书中使用EU REP 信息
2)修订和编制符合MDR 的CE技术文件
3)申报欧盟注册
4)指导企业编订符合声明:
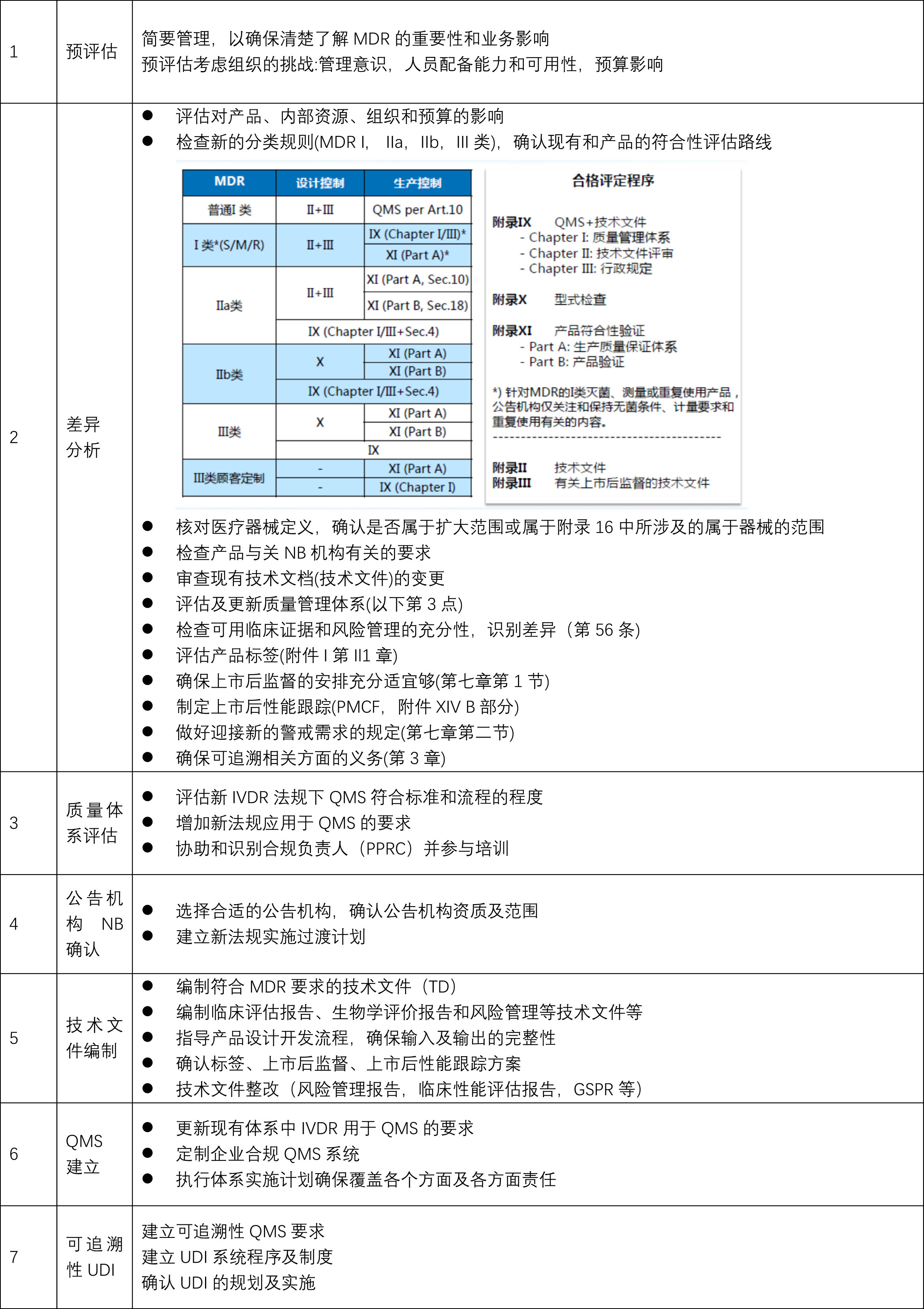
无论按照MDD指令或者MDR法规,口罩、隔离服等产品均属于I类产品。如果产品是非无菌的,根据MDD或MDR要求,I类非无菌医疗器械*公告机构介入。
I类非无菌产品出口欧盟要求:
1. 编制CE技术文档
2. 产品送检,取得产品检测报告
3. 出具自我符合性声明
4. 由欧代在其所在欧盟成员国主管当局(如CIBG、MHRA)进行信息注册并保存制造商的技术文档副件。
5. 在产品包装、标签上标记CE标志
2) I类无菌医疗器械:
若产品是I类无菌医疗器械,则需要公告机构介入,有一个较长的审核周期。
I类无菌医疗器械销往欧盟要求:
1. 编制产品技术文档
2. 建立ISO13485体系
3. 产品送检,取得产品检测报告
4. 接受公告机构的现场质量体系审核和技术文档审查
5. 获得具备相应资质的公告机构出具的CE认证证书
6. 由欧代在其所在欧盟成员国主管当局(如CIBG、MHRA)进行信息注册并保存制造商的技术文档副
7. 在产品包装、标签上标记带有公告机构号的CE标志
- “办理TUV机构的MDRCE认证需要做哪些检测?-需要什么材料”联系方式
- 我要给“办理TUV机构的MDRCE认证需要做哪些检测?-需要什么材料”留言
- “办理TUV机构的MDRCE认证需要做哪些检测?-需要什么材料”商家推荐产品
- 办理TUV机构的MDRCE认证需要做哪些检测?-需要什么材料相关产品