- 2024-04-30 11:02 712
- 产品价格:面议
- 发货地址:上海金山 包装说明:不限
- 产品数量:9999.00 个产品规格:不限
- 信息编号:286123758公司编号:14235332
- 袁小姐 经理 微信 13818104617
- 进入店铺 在线留言 QQ咨询 在线询价
纸尿裤的MDR-CE认证 MDR技术文档对CE认证的重要性
- 相关产品:
产地:上海可售地:**品牌:SUNGO型号:SUNGO BV包装:纸质
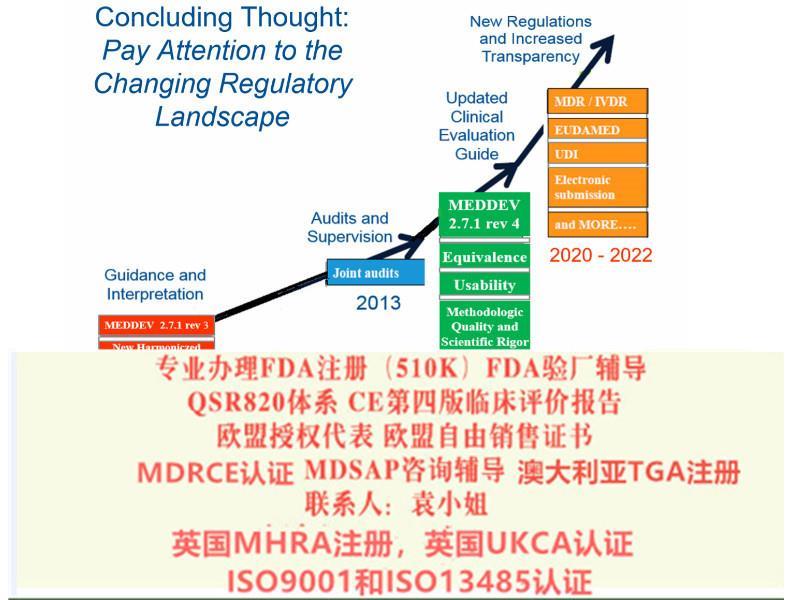
对制造商和产品的影响而言,93/42 EEC指令和MDR基本上具有相同的基本要求。没有现有的需求,但是MDR添加了新的需求,与目前93/42指令相比,MDR更加强调生命周期方法的性,并有数据支持。MDR对公告机构的提出了更严格的要求,对主管当局和会加强了控制和监测。MDR对某些设备重新分类,范围更广。例如,MDR明确涵盖用于清洁、或其他设备的所有装置(第2.1条);一次性器械(第17条)};和某些无用途的装置(附件十六)。MDR还包括在互联网上销售器械以及用于远程提供诊断或服务的器械(第6条)。MDR为一些Ilb类器械和植入性Il类器械引入了由立小组进行的评估咨询程序(第54条)。给企业一些建议:
•要求的大幅增加对制造商(特别是中小企业)产生了巨大影响
•增加人才**性:制造商,机构,组,欧盟授权代表等需要熟悉法规,技术和人员
•尽早开始准备!
•检查产品分类和合规途径是否受到影响!
•内部自我检查,以确保技术文件:符合的技术要求;特别是评估!满足语言要求
•了解MDR和内部差距分析的变化
•选择一个稳定,成熟的公告机构!
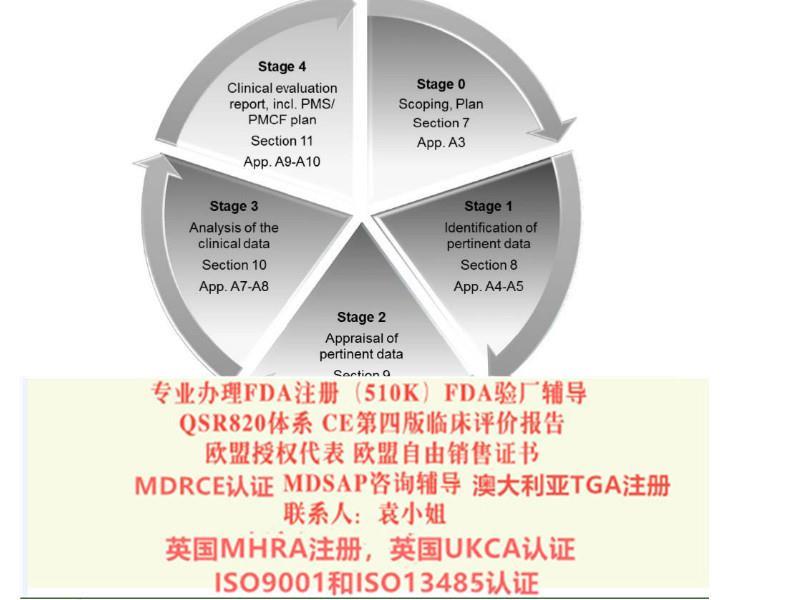
MDRCE认证,CEMDR认证,编写CE技术文件,CE第四版评价报告,(MDRCE技术文件:Medical Device Regulation 2017/745/EU)

SUNGO作为**化的器械法规技术服务商,可提供服务:
1. 确定您的器械在美国的具体分类及风险级别;
2. 企业准备510(k)申请所需的资料;
3. 确定检测标准及适用项目,推荐测试机构,对检测报告进行审查;
4. 编撰510(k)申报文件;
5. 企业进行小企业资质申请;
6. 跟踪510(k)文件评审进度;
7. 企业整改发补问题;
8. 进行企业注册和产品列名。

我们该怎么办?
重新确认产品风险分类等级,确认是否有风险等级升级的情况?
例如部分可重复使用的器械,原属于ClassⅠ的器械,按照新法规变成了ClassⅠ*类器械。美容类产品原MDD下不属于范围,现MDR法规中已纳入;
确认原CE证书的发证机构是否已获得欧盟当局批准的颁发MDR证书的资质,目前拥有该资质的认证机构:BSI、TUV南德(注意TUV莱茵目前还未获得批准);
确认原CE认证时的技术文件中是否含有按照Rev4原则提供的评价报告;
确定企业合规负责人(MDR法规要求),有相应能力、资质和经验来承担相应的法规工作职责。
修改原CE技术文件,建立质量管理体系,向具有MDR发证资质的认证机构提出MDR-CE认证申请,获得MDR法规下的新CE证书。
我公司办理:ISO13485认证,CE评估报告编写 等产品出口的相关认证